新闻纪录
[2023-08-07] 李卫/刘洪彬/季葆华/纪伟团队合作揭示精子鞭毛非对称性结构调控精子运动的作用机制。

近日,广州市妇女儿童医疗中心李卫团队、山东大学刘洪彬团队、浙江大学季葆华团队以及中科院生物物理所 纪伟团队共同在Current Biology杂志线上发表题为 CCDC176 stabilizes microtubule doublets 1 and 9 to ensure proper sperm movement 的研究型论文, 报道了精子鞭毛非对称性分布蛋白CCDC176调控精子运动的作用机制。
在该研究中,研究人员鉴定出了一个结构高度保守的卷曲螺旋结构域蛋白CCDC176, 发现其在小鼠睾丸中高表达并定位于精子鞭毛。为了研究其具体功能,研究人员构建了Ccdc176敲除小鼠模型, 结果发现Ccdc176敲除小鼠精子运动能力显著降低,产生弱精子症表型进而导致雄鼠不育。精子鞭毛结构透射电镜结果 发现Ccdc176敲除导致精子轴丝结构的1号及9号二联体微管特异性缺失,而这种精子鞭毛特异性微管缺失最早发生在附睾体处, 预示Ccdc176敲除不影响精子轴丝结构的组装而影响其稳定性维持。 为了明确CCDC176维持精子结构稳定的作用机制,作者利用新型干涉定位显微镜(ROSE-Z)检测了CCDC176在精子鞭毛中定位, 结果发现CCDC176在精子轴丝结构内部呈现周期性点状分布,且在精子轴丝中呈现非对称性分布。 进一步研究发现CCDC176可以与微管以及放射辐条相关蛋白结合,因此CCDC176在精子轴丝中非对称性分布并结合微管 以及放射辐条相关蛋白,在精子成熟过程中特异性维持1号及9号二联体微管的稳定。
近期对小鼠精子轴丝的冷冻投射电镜观察也发现放射辐条中存在非对称性分布结构,为了明确这些非对称性结构在精子运动中的功能, 作者构建了精子运动的力学模型。通过在精子运动过程中对精子轴丝结构9个二联体微管上的力学分析, 作者发现对称性结构会造成1号和9号二联体微管上应力显著增强。然而,根据冷冻投射电镜中的观察结果, 缩减1号和9号放射辐条的半径会显著降低1号和9号二联体微管上的应力,提高轴丝结构的稳定性,增加精子运动速度。 因此,精子轴丝中非对称性结构有利于提高精子运动速度及结构稳定性维持。
研究人员进一步利用该精子运动模型研究1号和9号二联体微管缺失对精子运动的影响, 结果发现1号和9号二联体微管缺失显著影响精子鞭毛摆动振幅和运动速度。 同时,1号和9号二联体微管缺失导致轴丝中央微管力矩降低并出现失衡, 进而导致精子呈现大范围的圆周运动。作者在Ccdc176敲除小鼠部分可运动的精子中观察到了类似现象。
综上所述,该论文鉴定出精子轴丝非对称性分布蛋白CCDC176,揭示了其在1号和9号二联体微管稳定性维持和精子运动中的调控基础, 明确了精子轴丝中非对称性结构在精子运动及结构稳定性维持中的功能,为人们研究和理解精子运动的力学基础提供了新思路。
[2023-04-20] 李卫团队构建新冠组织特异性感染小鼠模型。
自2019年底疫情爆发以来,动物模型在帮助快速开发预防和治疗疫苗/药物, 以及研究SARS-CoV-2感染的发病机制和宿主的免疫反应等方面发挥了至关重要的作用。
迄今为止已经开发了多个新冠动物模型,但在探讨不同组织中SARS-CoV-2病理机制时, 究竟是直接还是间接感染所导致的症状则很难分清。此外,以往的动物模型都只能在P3实验室操作,这极大地阻碍了人们对SARS-CoV-2的研究和抗击措施的开发。
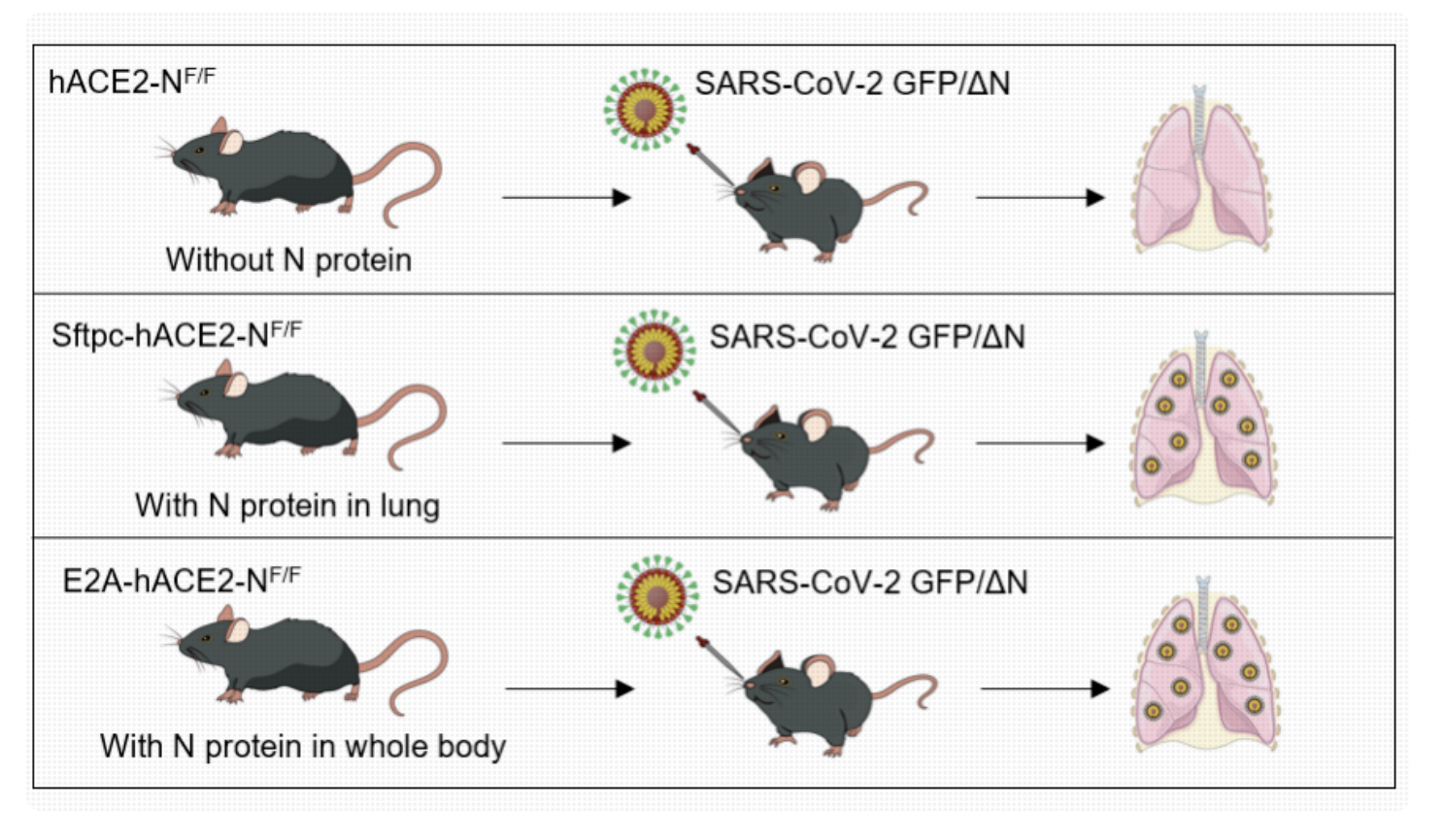
在前期开发了只能在表达SARS-CoV-2核衣壳(N)细胞中复制的SARS-CoV-2 trVLP(病毒样颗粒)系统基础上, 我们进一步利用Cre-loxP系统制备了能在小鼠特定组织中表达N蛋白和ACE2的小鼠品系。因为只能在遗传修饰过后的特定组织中感染和复制, 该小鼠模型可以在P2实验室环境下重现整个病毒生命周期。从而构建了新型冠状病毒的组织特异性感染小鼠模型,该小鼠模型支持不同的SARS-CoV-2变异株的感染, 可以用于评估治疗性单克隆抗体和抗病毒药物的抗病毒效果。
此外,该团队利用睾丸支持细胞特异感染模型证明SARS-CoV-2感染可导致睾丸组织血睾丸屏障的破坏从而导致生精障碍, 说明在某些特定条件下新冠的感染可能影响男性生殖系统。该论文于2023年4月20日以" A tissue specific-infection mouse model of SARS-CoV-2"为题在线发表于《Cell Discovery》杂志。
[2022-11-25] 优生围产研究所李卫团队建立睾丸电转技术结合自噬抑制剂治疗非梗阻性无精症的新途径。
近日,广州市妇女儿童医疗中心优生围产研究所李卫研究组联合广东省第二人民医院孙青原研究组在 Molecular Therapy - Nucleic Acids杂志上在线发表了题为Testis electroporation coupled with autophagy inhibitor to treat non-obstructive azoospermia的研究论文,揭示了通过睾丸曲细精管内显微注射后进行电转挽救了Rnf20敲除小鼠的精子 发生过程,并结合卵胞浆内单精子注射技术,使得非梗阻性无精子症小鼠产生了健康的子代。
该研究首先通过在睾丸注射和电转过程中尝试使用不同的载体和标签使RNF20质粒成功在小鼠睾丸中表达。 Rnf20敲除导致雄性小鼠精子发生过程障碍,为随后的研究提供了NOA小鼠模型。研究发现通过该NOA小鼠模型进行睾丸曲细精管内显微注射和电转挽救了年轻Rnf20敲除小鼠的精子发生过程。
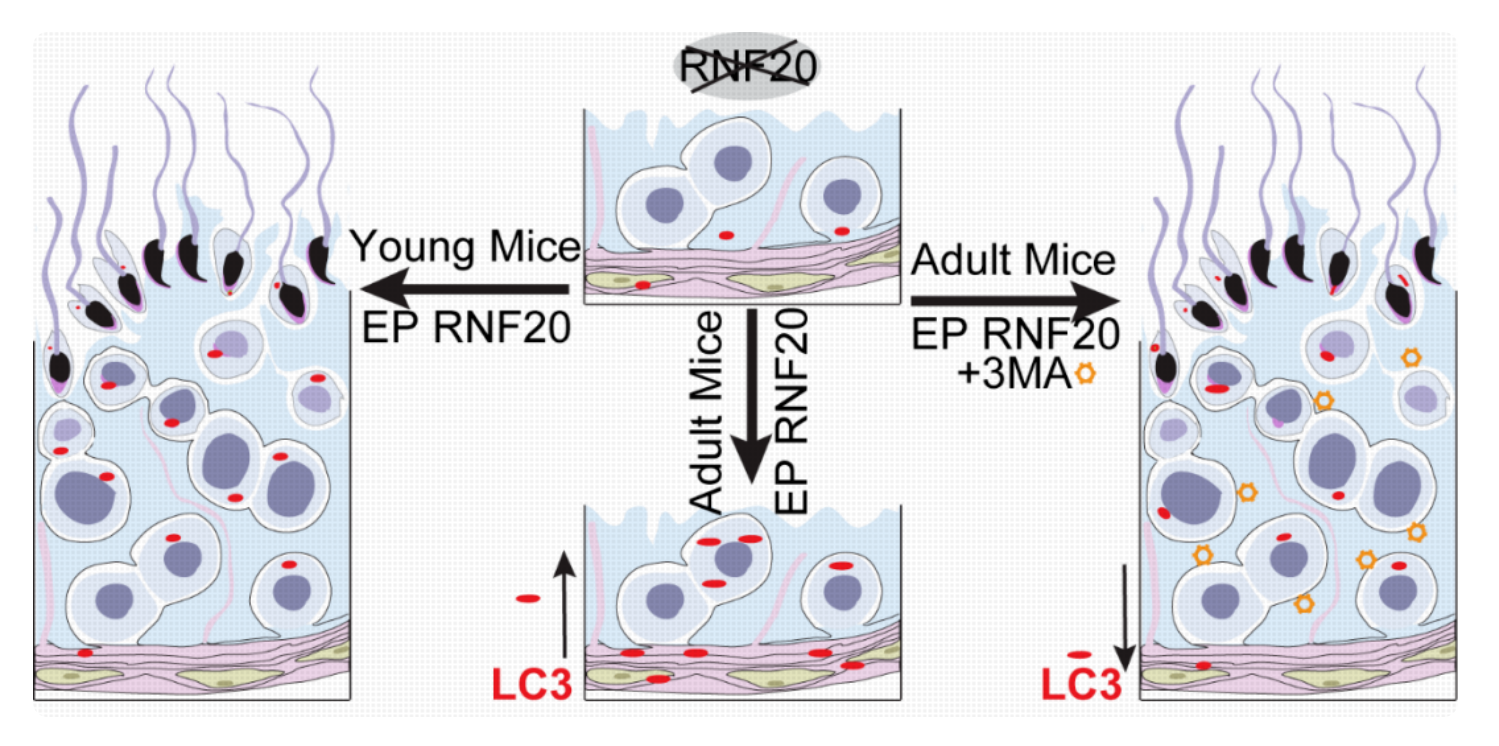
进一步的实验结果表明睾丸电转挽救了Rnf20敲除小鼠的减数分裂程序性 DSB 修复因子的招募和减数分裂粗线期阻滞, 最终挽救了敲除小鼠的精子发生过程。并且研究人员发现年轻小鼠睾丸中的电转效率高于成年小鼠,而无精子症往往在成年后才能被发现。由于睾丸是一种免疫豁免器官, 可能通过自噬作用对抗病原微生物,从而阻止外源DNA的表达。
为了证实这一猜想,研究人员通过在成年小鼠睾丸电转过程中加入自噬抑制剂(3-MA)显著提高了电转效率, 随后在成年Rnf20敲除小鼠中进行验证,研究结果发现在电转过程中加入低浓度的自噬抑制剂成功的挽救了成年Rnf20敲除小鼠的精子发生过程。由于精子浓度依然较低, 不能通过自然交配繁殖后代。后续结合卵胞浆内单精子注射技术,该NOA小鼠成功产生了健康的子代。
[2022-08-30] 优生围产研究所李卫等团队揭示原发性卵巢功能不全的潜在发病机理。
原发性卵巢功能不全 (Primary ovarian insufficiency, POI), 也称为卵巢早衰,是一种人类卵巢缺陷,其特征是 40 岁之前卵巢卵泡过早耗竭。然而,这种疾病的潜在机制仍然很大程度上未知。
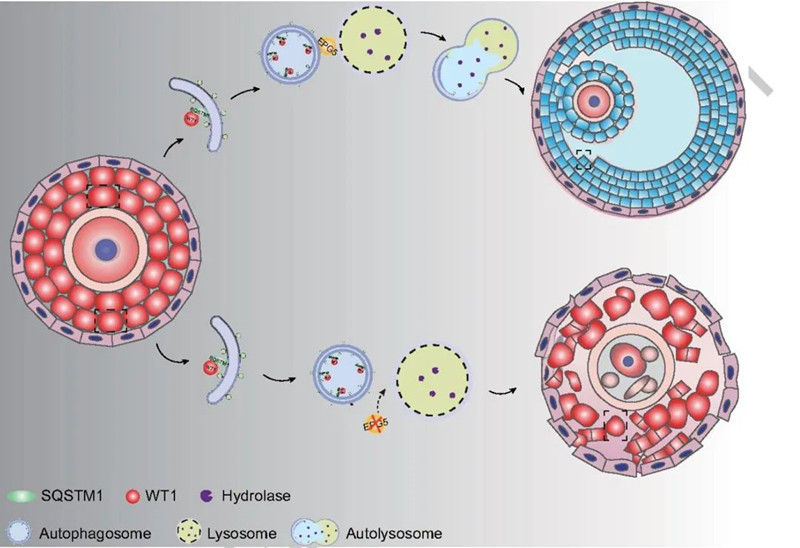
2022年7月27日,广州医科大学/中国科学院动物研究所李卫、 中国科学院动物研究所高飞和河南科技大学姜宏卫合作在Autophagy 杂志在线发表题为“Epg5 deficiency leads to primary ovarian insufficiency due to WT1 accumulation in mouse granulosa cells”的研究论文, 该研究发现敲除基因Epg5(ectopic P-granules autophagy protein 5 homolog(秀丽隐杆线虫)) 会导致雌性小鼠生育力低下,并表现出原发性卵巢功能不全样表型。单细胞RNA测序分析显示Epg5的敲除影响了颗粒细胞 (granulosa cells, GCs) 的分化。
进一步的研究表明,敲除 Epg5 会阻断自噬流(即细胞自噬发生的全过程), 导致WT1(WT1 转录因子)的积累,这是颗粒细胞的必需转录因子,表明WT1需要通过自噬途径被选择性降解。 并且在窦卵泡阶段WT1的不充分降解导致类固醇生成相关基因的表达降低,从而破坏了颗粒细胞分化。 总的来说,该研究表明EPG5促进颗粒细胞中的 WT1 降解,表明颗粒细胞中Epg5的失调引发原发性卵巢功能不全发病机制。
[2022-06-08] 广州市妇儿中心联合多家团队揭示部分COVID-19患者 肺部损伤和嗅味觉丧失的可能机制。
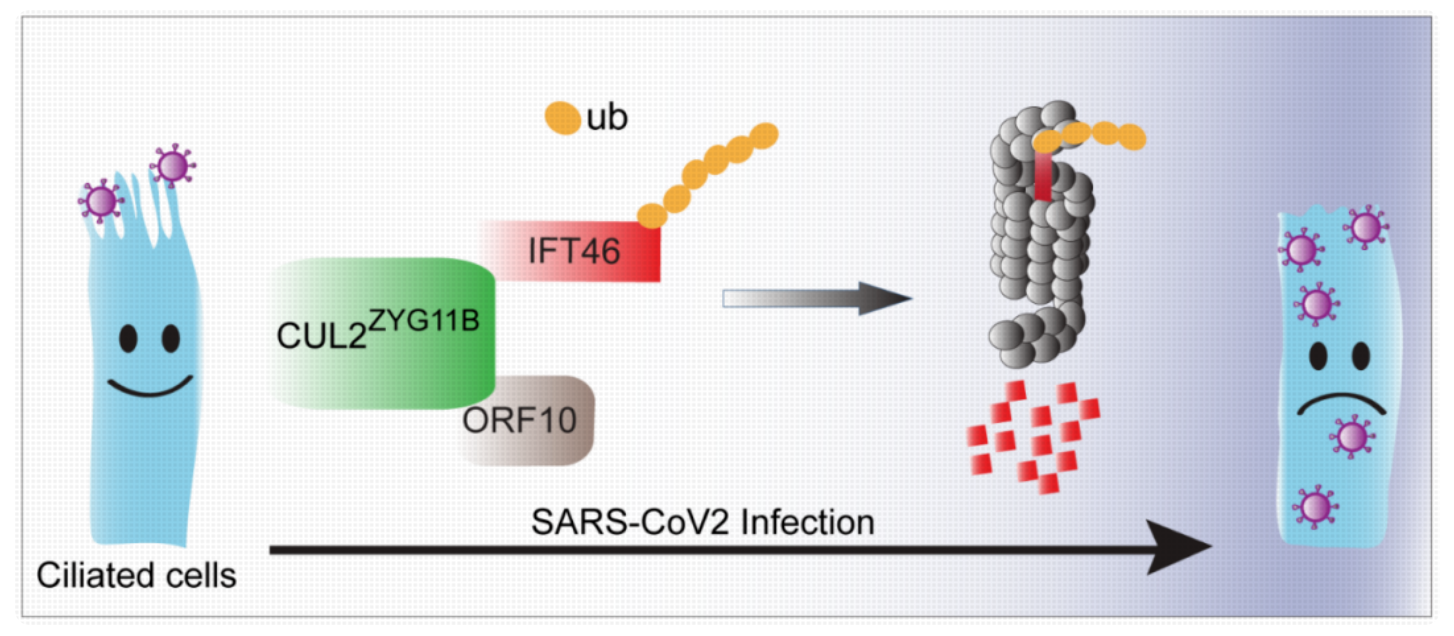
2022年6月8日,广州市妇女儿童医疗中心优生围产研究所李卫研究组联合南京医科大学郭雪江研究组, 中国科学院动物研究所实验动物中心多曙光博士,北京市耳鼻咽喉科研究所张罗研究组在Journal of Cell Biology杂志上在线发表了题为 SARS-CoV-2 ORF10 impairs cilia by enhancing CUL2ZYG11B activity的研究论文,揭示了SARS-CoV-2 ORF10通过促进 CUL2ZYG11B泛素连接酶的活性, 加速鞭毛转运蛋白IFT46的降解,从而破坏纤毛组装和功能维持的作用机制。
该研究发现ORF10能够直接结合ZYG11B促进CUL2ZYG11B E3连接酶活性。 质谱结果发现ORF10的表达导致纤毛相关蛋白表达下调。进一步的实验结果表明CUL2ZYG11B 通过和细胞纤毛内转运蛋白IFT46的C2结构域 相互作用从而促进IFT46的泛素化修饰介导其通过蛋白酶体进行降解,从而破坏纤毛的组装和维持。
为了进一步证实SARS-CoV-2 ORF10影响纤毛组装和维持的作用机制,研究人员通过在hACE2小鼠模型和原代人鼻上皮细胞(HNECs) 中感染SARS-CoV-2 ORF10表达腺病毒,检测ORF10表达对小鼠呼吸道和人多纤毛细胞的影响。
结果显示hACE2小鼠呼吸道感染SARS-CoV-2 ORF10腺病毒后导致气管纤毛丢失,ORF10在HNECs细胞中的表达也导致多纤毛丢失。进一步利用SARS-CoV-2感染hACE2小鼠, 也可以导致小鼠气管纤毛损伤,从而证实了SARS-CoV-2导致纤毛功能障碍的调控机制。

 官方微博
官方微博